ノババックス社製ヌバキソビットについて 2023.1.20
![]()
ヌバキソビッド(ノババックス社製の遺伝子組換え蛋白ワクチン)
1)開発元
アメリカノババックス社が開発したワクチンを、武田薬品が承認申請を行い、2022年4月19日に薬事承認されました。2022年5月下旬から、我が国でも使用されています。
2)作用機序
ヌバキソビッドは、新型コロナウイルスSARS-CoV-2のスパイク蛋白(コロナウイルスのトゲの部分の蛋白。コロナウイルスのスパイクはヒト細胞のリセプターにくっついて、ヒト細胞内に侵入するために必要な働きをします。下図左)と、免疫を増強するためのMatrix-M1アジュバント(サポニンとコレステロール、ホスファチジルコリンで作られたケージ状粒子。下図右)を併せ持つ、遺伝子組換え蛋白ワクチンです。
 |
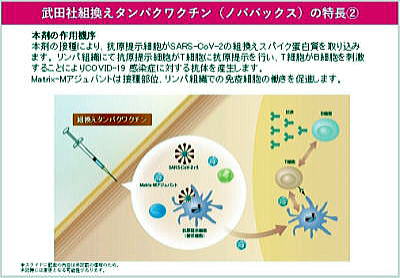 |
| 左はナノ粒子を囲んで集合したスパイク蛋白。右はサポニン、コレステロール、脂質のアジュバンド。(第31回 厚生科学審議会予防接種・ワクチン分科会資料より引用) | 本剤の接種により組換えスパイクタンパク質がヒトの細胞内に取り込まれると、スパイクタンパク質に対する中和抗体産生及び細胞性免疫応答が誘導されることで、SARS-CoV-2による感染症の予防ができる。(引用は左と同じ) |
バキュロウイルス(蝶の幼虫に感染する、DNAウイルスでヒトに病原性はありません。)にコロナウイルスのスパイク蛋白の遺伝子情報を組み込み、このウイルス昆虫細胞に感染させて、昆虫細胞にコロナウイルスのスパイク蛋白(抗原)を作らせます。この抗原蛋白を、脂質(ポリソルベート80)を核に集合させて粒子にして、ヒトに接種します。
mRNAワクチンがRNAをヒト細胞に接種するのに対し、組換え蛋白ワクチンは昆虫細胞に作らせた蛋白を接種することが異なります。
接種されたスパイク蛋白は免疫細胞(抗原提示細胞)に取り込まれ、異物(敵)として認識され、この情報は免疫司令官Tリンパ球に伝達されます。Tリンパ球はBリンパ球に指令を出し、Bリンパ球は中和抗体を産生し、スパイク蛋白を持つコロナウイルスを攻撃します。
同時に注入された、サポニンのMatrix-M1アジュバントは、免疫組織の働きを促進します。
この遺伝子組換え蛋白ワクチンは不活化ワクチンの一つで、B型肝炎ワクチンと同じグループに属します。(①ワクチンの種類、Ⅱ不活化ワクチン参照)
3)接種の方法
2022年5月下旬から接種可能になりました。初回接種にも追加接種にも使用できます。
①初回接種:3週間間隔で2回、ヌバキソビッド0.5mlを筋肉注射します。対象は12歳以上です。
②追加接種:初回接種後、6ヶ月以上あけて、ヌバキソビッド0.5mlを1回筋肉注射します。対象は12歳以上です。
4)効果と副反応
オミクロン株流行前の臨床検討では、コミナティやスパイクバックスなどのmRNAワクチンよりは効果が劣るものの、ウイルスベクターワクチンであるバキスゼブリアよりは有効だったようです。
また、副反応については現在の検討結果では、重い症状は報告されていません。同じグループであるB型肝炎ワクチンが、ほとんど重篤な副反応がみられないことから、重い副反応が今後報告される可能性は少ないものと思われます。
諸外国での検討結果を示します。
①ヌバキソビッド0.5mlを、3週間隔で2回、筋肉注射した検討(初回接種)
アメリカ、メキシコで行われた、18歳以上を対象とした臨床試験の結果では、ヌバキソビッド初回接種後約3か月における発症予防効果は、90.4%と報告されています。(2020年12月~2021年2月実施)
また、接種後7日目までの副反応は軽度~中等度で、追跡期間中に安全性の懸念は認められなかったと報告されました。
Dunkle LM,Kotloff KL, Gay CL, et al. Efficacy and Safety of NVX-CoV2373 in Adults in the United States and Mexico. N Engl J Med. 2022;386(6):531-543.
②ファイザー、アストラゼネカワクチンを2回接種した後に追加接種した結果の検討
ヌバキソビッドを初回接種ではなく、コミナティ(ファイザー)やバキスゼブリア(アストラゼネカ)を接種した後、3回目として追加接種した効果の臨床研究です。
30歳以上を対象としたこの試験の結果は、初回接種でファイザーワクチン又はアストラゼネカワクチンを接種した後に、ヌバキソビッドを追加接種した場合(交互接種)でも、中和抗体価は被接種対照群と比較して有意に上昇し、副反応についても安全性は許容される範囲であったと報告されました。
Alasdair P S Munro,et al:Safety and immunogenicity of seven COVID-19 vaccines as a third dose (booster) following two doses of ChAdOx1 nCov-19 or BNT162b2 in the UK (COV-BOOST): a blinded, multicentre, randomised, controlled, phase 2 trial ;Lancet.2021;398, I2258-2276
5)当クリニックの評価
mRNAワクチンで副反応が強かった人、mRNAワクチンを打ちたくない人対象のワクチンとして、位置付けられています。
当クリニックは、初回接種にはmRNAワクチンの方が効果が期待されるため、mRNAワクチン接種を推奨します。しかし成人の追加接種には、本ワクチン=ヌバキソビッドが適当と考えます。
現在、品川区では品川区医師会館のみで接種が行われています。
品川区のお知らせ:武田社ワクチン(ノババックス)の接種について
厚労省:初回(1.2回目)接種案内の説明書
厚労省:追加(3.4.5回目)接種案内の説明書
参考文献・サイト:
第31回 厚生科学審議会予防接種・ワクチン分科会資料
厚労省:武田薬品工業株式会社の新型コロナワクチンについて
大岩ゆり:ノババックス製ワクチンの特徴は? ファイザー、モデルナとどう違う ?;Reライフ・ネット
![]()