新型コロナワクチン各論
2022.11.20更新
![]()
①ファイザー社製メッセンジャーRNAワクチン
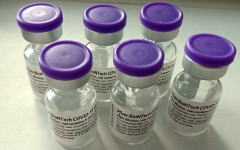
1)開発元
ドイツの遺伝子医薬品開発ベンチャー企業だったビオンテック社とアメリカの製薬企業ファイザーが、共同で開発したmRNA(メッセンジャーRNA)ワクチンです。
アメリカでは、2020年12月11日に緊急使用が認可され、我が国でも、2021年2月15日、特例承認されました。
現在、従来株ワクチン、小児用ワクチン、乳幼児用ワクチン、オミクロン株対応2価ワクチン(BA.1対応、BA4/5)と4種類の製剤が認可されています。まず、その働きをみた後、それぞれのワクチンの説明をいたします。
2)作用機序
新型コロナウイルスが細胞に侵入するときに、細胞に密着するスパイクと呼ばれる糖蛋白(ウイルスから出ているトゲの蛋白質)を設計する情報を持ったmRNA(メッセンジャーRNA)を、脂肪の膜である脂質ナノ粒子で包み込んで、ヒトに接種するmRNAワクチンです。
ヒト体内に注入されたmRNAが、ヒト体内の細胞質でヒトの成分を使って、SARS-CoV-2のスパイク蛋白を作ります。ところがこのウイルススパイク蛋白はヒトにとって異物のため、免疫が誘導されます。
ただし、この作成されたウイルスのスパイク蛋白自体は無害です。また、このスパイク蛋白が作られた後、ワクチンのmRNAはヒトの細胞で処理されて、数時間で破壊されます。mRNAがヒト体内に長く留まることはありません。
また、このmRNAはヒト細胞の細胞質リボゾームでスパイク蛋白を作り出しますが、ヒト細胞核内に侵入することは出来ないので、ヒトの遺伝子情報そのものが影響されることはありません。(ワクチン総論、核酸ワクチンもご参照ください。)
現在、ファイザー社製のワクチンは、今使われているファイザーワクチン(武漢株の1価ワクチン)、小児用コロナワクチン(ワクチン成分を減量してある、子ども用の武漢株の1価ワクチン)、オミクロン株対応2価ワクチン(BA.1対応、まもなくBA4/5対応が登場予定)の3種類あります。
それぞれ個別に説明いたします。
Ⅰ.コミナティ筋注:武漢株=従来株の1価ワクチン
現在ファイザーワクチンとして、最も多く接種されているワクチンです。
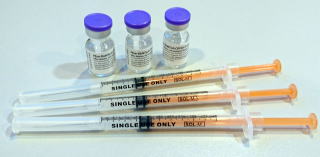 3)接種方法
3)接種方法
コミナティ筋注は、21日間隔(3週間)で、上腕三角筋に0.3mlを2回筋肉注射します。
発症予防効果は、2回目接種後7日~2ヶ月未満では96.2%でしたが、4ヶ月以降では83.7%と低下していました。(デルタ株以前のデータ)
そのため、現在3回目の追加接種が行われるようになりました。 (→コロナワクチン3回目接種についてはこちらをお読みください。)
さらに4回目も行われるようになりました。(4回目接種についても、こちらをお読みください。)
他のワクチンとの同時接種はできませんでしたが、インフルエンザワクチンのみは同時接種が認められました。したがって、コミナティ筋注を接種した前後14日間は、インフルエンザワクチンを除く他のワクチンの接種は控えます。(インフルエンザワクチンのみは間隔を考慮せず、接種できます。)
さらに2回接種後の、3回目の追加接種は同じmRNAワクチンのスパイクバックス(モデル社製ワクチン)、ヌバクソビッド(ノババックス社製コロナワクチン)の接種も認められています。
コミュニティ筋注は、1、2、3、4回目接種とも、0.3mlを筋肉注射します。
4)ワクチンの効果
このファイザーワクチンの第3相試験は、2020年7月からアメリカ、ブラジル、アルゼンチン、南アフリカ、ドイツなどの154施設で開始され、43538例が登録され、38955例が2回ワクチンの接種が行われました。解析結果は、ワクチンの発症予防効果は95%と報告されました。
一方、デルタ株については、発症予防効果は88%と報告されています。
オミクロン株に対しては、
5)ワクチンの対象
12歳以上が接種対象になります。
6)ワクチンの副反応
局所症状として、接種部位の痛み、腫れ、赤くなる、接種した側の脇の下のリンパ節の腫れがみられます。
全身症状として、発熱、全身のだるさ、頭痛、寒気、筋肉痛、関節痛がみられます。
即時型反応(接種4時間以内に起こる、じんましん、むくみ、ぜいぜい、アナフィラキシーなど)の発生率は0.63%、プラセボ(ワクチンに似せた生食水など)では0.51%と報告されています。
これらの副反応は接種後3日以内に起こり、多くは1~2日の経過で消失すると報告されています。また、1回目より2回目の方が、また55歳以上より18歳~55歳の方が多く起るようです。
ただし接種によって副反応が起きたとしても、新型コロナウイルスワクチン接種でアナフィラキシーショックのような重い症状が出た人、ポリエチレングリコール(PEG)やポリソルビートに重大なアレルギー歴のある人*で無ければ、2回目の接種は可能です。
*このような体質の人は、ワクチンに封入されている脂質ナノ粒子(LNP)にアレルギー反応を起す可能性があるためです。
mRNAワクチンは、他のワクチンと比較しても、接種後の副反応が強く表われます。注射の痛みは、最も痛いと評価されてきたプレベナー13やニュ-モバックスと同等か、それ以上と報告されています。
心筋
Ⅱ.小児用ワクチン:コミナティ筋注5~11歳用(くわしくは、こちら)
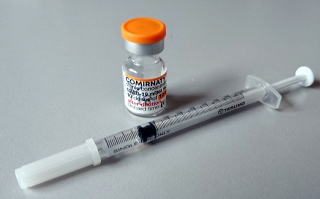 3)製品と接種の方法
3)製品と接種の方法
一方、小児用コロナワクチンは、21日の間隔(3週間)をあけて、2回上腕三角筋に0.2mlを注射します。
小児用コロナワクチンは今の所、3週間隔で2回接種で終了となっていますが、オミクロン株に対し、3回接種で発病予防効果が上昇することがわかっているため、いずれ3回目の接種が行われることになると思われます。
4)ワクチンの効果
5)ワクチンの対象
小児用コロナワクチンは5歳~11歳が対象です。
6)ワクチンに副反応
成人用(従来株)ワクチン(コミナティ)に比較して、副反応は少ないと言われています。
3)2価ワクチン
②モデルナワクチン(スパイクバックス:モデルナ社製のmRNAワクチン)
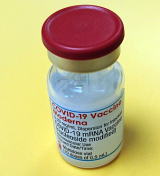
1)開発元
アメリカの遺伝子医薬開発ベンチャー企業のモデルナ社とアメリカ国立アレルギー・免疫研究所が共同で開発した、mRNAワクチンです。
アメリカでは2020年12月18日に緊急使用が許可され、イギリスでは2021年1月8日に通常認可されています。
我が国では2021年5月21日に初回接種(2回)が特例承認されました。追加接種については、2021年12月16日に薬事承認されました。
*認可当初は、「COVID-19ワクチンモデルナ筋注」という名称でしたが、2021年12月16日、「スパイクバックス筋注」と変更されました。
2)作用機序
コミナティと、同じmRNAワクチンのため、作用機序も同じです。(作用機序については、こちらをご覧下さい。)
3)接種の方法
初回接種(1回目、2回目)は、28日(4週間)の間隔を開けて、1回0.5mlを2回、上腕三角筋に筋注します。(対象は12歳以上。)
追加接種(3回目)は、初回接種後6週間以上あけて、1回0.25ml(初回接種量の半量)を上腕三角筋に筋注します。(ただし、対象年齢は18歳以上となっています)
初めの2回は、原則同じワクチンを接種します。3回目の追加接種は他のワクチンの接種(たとえば、コミナティ)も認められています。(例えば、モデルナ-モデルナ-ファイザー。)
他のワクチンとの同時接種はできません。また、モデルナのワクチン(スパイクバックス)を接種した前後14日間は、他のワクチンの接種は控えます。
![]() 非常に間違えやすい、複雑な設定になっています。スパイクバックスでは初回2回と追加3回目は、接種量も接種年齢も異なります。接種ミスを減らすよう、なるべく単純化(年齢、接種量)しようという配慮は、お役人には全くありません。ただただ、厚労省も保健所も注意するよう、通達を出すだけです。間違いでもしたら、「医療機関で誤接種!」とマスコミに通報され、さらし者にされます。
非常に間違えやすい、複雑な設定になっています。スパイクバックスでは初回2回と追加3回目は、接種量も接種年齢も異なります。接種ミスを減らすよう、なるべく単純化(年齢、接種量)しようという配慮は、お役人には全くありません。ただただ、厚労省も保健所も注意するよう、通達を出すだけです。間違いでもしたら、「医療機関で誤接種!」とマスコミに通報され、さらし者にされます。
ワクチンの有効期限も変更になりました。ワクチンバイアル、シールに貼ってある有効期限を越えて、接種が行われています。(厚労省の発表)
接種間隔も朝令暮改でころころ変えられています。3回目の接種間隔も、8ヶ月→6ヶ月→5ヶ月と変更されました。そのたびに、「期間を間違えると誤接種になるぞ。」と脅しの文句が医療機関に回ってきます。
医療機関の側も、コロナ対応だけでも大変なのに、このような(本来あまり問題とならないような)複雑極まりないルールを遵守し、接種するときにミスにならないよう細心の注意を払うなど、その精神的重圧は凄まじいものがあります。
4)ワクチンの効果
モデルナのmRNAワクチンの有効成分エラソメランの方が、ファイザーのmRNAワクチンの有効成分トジナメランよりも量が多いため、効果も強いが、副反応も強いようです。
▷18歳以上
<海外における臨床試験>
アメリカにおいて、約3万人の被験者を対象に、2回目の接種後14日以降の発症の有無が比較されました。その結果、過去に新型コロナウイルスの感染歴がない被験者において、94.1%のワクチン有効率が確認されました。(オミクロン流行前の研究です)
<国内における臨床試験>
日本人の健康成人200人をワクチンとプラセボ(生食水などのにせのワクチン)に分け、約28日間の間隔で2回接種しました。そして、2回目の接種から28日後の、接種した人のコロナウイルスに対する血液中の抗体を調べた所、抗体価の上昇が確認されました。
▷12~17歳
<海外における臨床試験>
12~17歳の約3000人の健康人を対象に、ワクチンとプラセボ(生食水などのにせのワクチン)に分け、約28日間の間隔で2回接種した時の、新型コロナウイルス感染症の発症がどの程度抑えられるか、比較しました。
2回目の接種後14日以降の発症について、過去に新型コロナウイルスの感染歴がない被験者では、100.0%のワクチン有効率が確認されました。
▷追加接種(3回目接種)の効果
<海外における臨床試験>
アメリカにおいて、18歳以上の人に、2回目の接種から6か月以上あけて、3回目のワクチン接種を行いました。接種した1か月後に、血液中の新型コロナウイルスに対する抗体を調べました。
1、2回目にエラソメラン100μgを接種した人に、3回目50μgを接種したところ、3回目接種の人で高い抗体価が得られました。
4)ワクチンの副反応
副反応については、こちらもお読みください(ワクチンの副反応参照)。
5)ワクチンの対象
1,2回の初回接種は12歳以上、3回目は18歳以上が対象です。
6)問題点
コミナティのように、-75℃という超低温で管理する必要がなく、流通・管理はコミナティに比べてはるかに楽です。モデルナワクチンは普通の冷蔵庫(2~8℃)で30日、品質は安定しており、-20℃なら6ヶ月間保存できるようです。
また、コミナティのように希釈精製することなくバイアルから吸い取るだけなので、操作が簡単なため、集団接種に適しています。
集団での接種に向いているので、集団接種、職域接種に使用されましたが、副反応が強いこと、特にモデルナアームや心筋炎などが警戒されたためか、接種希望者は少ないようです。
![]() 各地方自治体では、続々廃棄処分のなるようです。あの大騒ぎは何だったのでしょうか。(報道の一例)
各地方自治体では、続々廃棄処分のなるようです。あの大騒ぎは何だったのでしょうか。(報道の一例)
③アストラゼネカのワクチン(バキスゼブリア:アストラゼネカ社製のウイルスベクターワクチン)
 1)開発元オックスフォード大学とイギリスの製薬企業アストラゼネカ社が共同で開発した、ウイルスベクターワクチン(遺伝子組換え)です。我が国では、2021年5月21日に特例承認され、8月3日臨時接種の使用ワクチンに追加されました。
1)開発元オックスフォード大学とイギリスの製薬企業アストラゼネカ社が共同で開発した、ウイルスベクターワクチン(遺伝子組換え)です。我が国では、2021年5月21日に特例承認され、8月3日臨時接種の使用ワクチンに追加されました。
2)作用
バキスゼブリア(アストラゼネカのワクチン)はウイルスベクターワクチンと呼ばれます。正式名称は、遺伝子組換えサルアデノウイルスベクターワクチンといいます。
このワクチンは、mRNAワクチンのように、病原ウイルスの蛋白を作るmRNAを、そのままヒト体内に直接注入するものではありません。
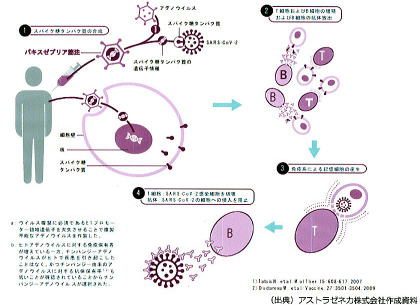 右図に示したように、チンパンジーのアデノウイルスなど、新型コロナウイルスと無関係な他のウイルスを、増殖できないように処理した上で、新型コロナウイルスのトゲ(スパイク)の断片を作る遺伝子情報を組み込みます。
右図に示したように、チンパンジーのアデノウイルスなど、新型コロナウイルスと無関係な他のウイルスを、増殖できないように処理した上で、新型コロナウイルスのトゲ(スパイク)の断片を作る遺伝子情報を組み込みます。
そして、人に接種します。
ヒト体内に注入されたウイルスは、新型コロナウイルスのとげの蛋白(スパイク蛋白)を持っているため、ヒト細胞内に侵入した後、ヒトの細胞成分を勝手に使って、新型コロナウイルスのスパイク蛋白を作り始めます。
このトゲの蛋白(スパイク蛋白)は細胞表面に顔を出し、免疫担当細胞によって異物(敵)として認識され、免疫反応が誘導されることになるのです。
サルアデノウイルスは、新型コロナウイルスの遺伝子をヒトに運搬するだけの役割のため、ウイルスベクター(運び屋=ベクター・ウイルス vector)と呼ばれます。
*上図は、2021年5月21日厚生科学審議会予防接種・ワクチン分科会提出資料から転載
*アストラゼネカ:アデノウイルスベクターワクチンの製造(動画)
3)接種方法
8週から12週の間隔で2回、上腕三角筋に1回0.5mlのワクチンを筋肉注射します。
*標準的には、27日(1ヶ月)から83日(3ヶ月)の間に行うとされています。すなわち、4週以上あければ接種は可能ですが、2回目は2ヶ月後がよいと思います。
最初の2回は同じバキスゼブリアを接種することが必要です。(mRNAワクチンとは作用が違うため)
接種年齢は18歳以上となっていますが、血栓症などのリスクを考えると、40歳以上が推奨されています。
4)ワクチンの効果
本ワクチンの接種を受けた人は、臨床試験の結果では、約70%等の発症予防効果が確認されました。
5)ワクチンの副反応
局所症状としては、注射部位の腫脹発赤、内出血、痛みやかゆみ、接種した側の脇の下のリンパ節の腫れなどが報告されています。
全身の症状としては、疲労、頭痛、倦怠感(だるさ)、筋肉痛、発熱感、悪寒、関節痛、吐き気などがみられます。
これらは、接種したときから出現し、1~3日以内に治まる事が多いです。また、1回目の方が2回目より副反応が出やすいようです。
(バキスゼブリアの副反応)
バキスゼブリアで特に問題となる副反応は、①血栓症と②毛細血管漏出症候群、③ギランバレー症候群です。
①血小板減少症を伴う血栓症(TTS:Thrombosis with Thrombocytopenia Syndrome)
バキスゼブリア接種後の、きわめてまれですが、もっとも重大で警戒すべき合併症です。
2021年4月に、血小板減少を伴う血栓症(TTS)を欧州医薬品庁(EMA)は「非常にまれな副反応」と認定しました。
TTSの特徴は、
1)バキスゼブリア接種後4~28日に起る、
2)脳静脈や内臓静脈など、普通はあまり起らない場所の小血管に小さな血の塊(血栓)が生じ、組織に深刻な障害を起す、
3)血小板が著しく減少し、身体の出血凝固系に異常を生ずる、5)抗血小板第4因子抗体(ELISA法)が陽性となるという免疫異常が起る、が挙げられます。
TTSの頻度は、100万人に15人と極めてまれですが、これまでに報告されたTTSは、出血や著明な脳浮腫を伴う重症脳静脈の血栓症が多く、死亡率も高いです。
原因はよくわかっていませんが、ワクチン接種によって、何らかの血小板に対する異常な免疫反応が起るためと考えられています。
TTSの症状は、激しい頭痛が続く、目のかすむ、息切れ、胸痛、錯乱、けいれん、胸の痛み、足のやむくみや痛み、持続する腹痛、接種部位以外の内出血(あざ)などが挙げられています。これらの症状がみられれば、すぐ受診する必要があります。
2回目の接種後よりも1回目の接種後に起きることが多いとされています。
②毛細血管漏出症候群(capillary leak syndrome):からだの毛細血管から液体が漏み出し、手足のむくみ、低血圧などの症状が起こり、全身の浮腫や腎不全などを引き起こす、非常に珍しい病気です。
ワクチン接種とこの病気の関連ははっきりしませんが、この病気にかかったことのある人がバキスゼブリアを接種すると毛細血管漏出を起すリスクのあるため、接種は受けられません。
③ギランバレー症候群:手足の力が入りにくい、歩けなくなる、腱反射が出なくなるなどの症状がでる神経の病気です。バキスゼブリア接種でギランバレー症候群が稀に起ります。
6)ワクチンの対象
原則、40歳以上の成人が対象となりました。(一応、18歳以上は接種可能です。)
1.18歳以上の方で次のいずれかに該当する者
・ポリエチレングリコール(PEG)に対するアレルギー等で、mRNAワクチンを接種できない人
・海外ですでにバキスゼブリアを1回接種している日本在住の人
2.40歳以上で、バキスゼブリアの接種を希望する人
7)問題点
当初は、冷凍が必要ないこと(通常のワクチンの取り扱いで良いこと)、小分けが可能なこと、価格が比較的安価なことなどから広く使用されることが期待されました。
しかし、mRNAワクチンに比べて効果が劣ること、血栓症のような重い副反応の報告があること、オミクロン株に効果が低いことなどから、あくまで使用されなくなりました。
参考文献・サイト
厚労省:アストラゼネカ社の新型コロナワクチンについて
MHRA:Vaxzebriaの製品特性の概要
④ノババックスワクチン(ヌバクソビッド:ノババックス社製の遺伝子組換え蛋白ワクチンワクチン)
1)開発元
アメリカノババックス社が開発したワクチンを、武田薬品が承認申請を行い、2022年4月19日に薬事承認されました。
(写真は、EPR:Novavax begins Phase III COVID-19 vaccine efficacy trial)
2)作用機序
ヌバクソビッドは、新型コロナウイルス=SARS-CoV-2のスパイク蛋白(コロナウイルスのトゲの部分の蛋白。スパイクはヒト細胞のリセプターにくっついて、ウイルスがヒト細胞内に侵入するために必要な働きをします。下図左)と、免疫を増強するためのMatrix-M1アジュバント(サポニンとコレステロール、ホスファチジルコリンで作られたケージ状粒子。下図右)を併せ持つ、遺伝子組換え蛋白ワクチンです。
 |
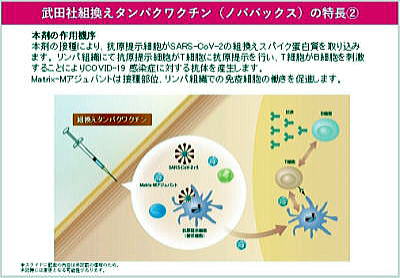 |
| 左はナノ粒子を囲んで集合したスパイク蛋白。右はサポニン、コレステロール、脂質のアジュバンド。(第31回 厚生科学審議会予防接種・ワクチン分科会資料より引用) | 本剤の接種により組換えスパイクタンパク質がヒトの細胞内に取り込まれると、スパイクタンパク質に対する中和抗体産生及び細胞性免疫応答が誘導されることで、SARS-CoV-2による感染症の予防ができる。(引用は左と同じ) |
バキュロウイルス(蝶の幼虫に感染する、DNAウイルスでヒトに病原性はありません。)にコロナウイルス・スパイク蛋白の遺伝子情報を組み込み、昆虫細胞に感染させて、昆虫細胞にコロナウイルスのスパイク蛋白(抗原)を作らせます。この抗原を、脂質(ポリソルベート80)を核に集合させて粒子にして、ヒトに接種します。
mRNAワクチンがRNAをヒト細胞に接種するのに対し、組換え蛋白ワクチンは昆虫細胞に作らせた蛋白を接種します。
接種されたスパイク蛋白は免疫細胞(抗原提示細胞)に取り込まれ、異物(敵)として認識され、この情報は免疫司令官Tリンパ球に伝達されます。Tリンパ球はBリンパ球に指令を出し、Bリンパ球は中和抗体を産生し、スパイク蛋白を持つコロナウイルスを攻撃します。
同時に注入された、サポニンのMatrix-M1アジュバントは、免疫組織の働きを促進します。
この遺伝子組換え蛋白ワクチンは不活化ワクチンの一つで、B型肝炎ワクチンと同じグループに属します。
3)接種の方法
①ヌバクソビッド 0.5mlを、3週間隔で2回、肩三角筋に筋肉注射します。(1回目、2回目接種)
12歳以上対象。1回目と2回目は同じワクチンで接種を受けます。
ただし、1回目のmRNAワクチンの副反応が強かった場合、医師の判断で2回目をヌバクソビッドに変更することは可能です。
②ヌバクソビッド 0.5mlを、2回目接種から6ヶ月あけて、肩三角筋に筋肉注射します。(3回目接種)
18歳以上対象。1回目、2日目は、ファイザー、モデルナワクチンでも、ノババックス(ヌバクソビッド)もかまいません。
4)問題点
オミクロン株流行前の臨床検討では、コミナティやスパイクバックスなどのmRNAワクチンよりは効果が劣るものの、ウイルスベクターワクチンであるバキスゼブリアよりは有効だったようです。
また、副反応については、現在重い症状は報告されていません。同じグループであるB型肝炎ワクチンも、ほとんど重篤な副反応がみられないことから、重い副反応が今後報告される可能性は少ないものと思われます。(ヌバクソビッドの副反応)
5)我が国での接種状況
9月から接種可能になると思われるので、mRNAワクチンで副反応が強かった人、mRNAワクチンを打ちたくない人用のワクチンとして、少数使われていくと思われます。
参考文献・サイト:
第31回 厚生科学審議会予防接種・ワクチン分科会資料
![]()